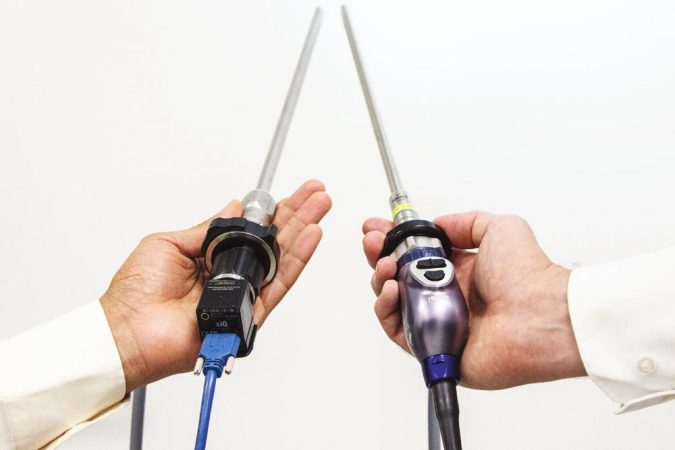
Minimalinvasive Operationstechniken, auch als „Schlüsselloch-OP“ bekannt, ersetzen zunehmend klassische offene Operationen – auch in der Krebsmedizin. So können beispielsweise bestimmte Tumoren der inneren Organe im Zuge einer Bauchspiegelung entfernt werden. Dabei kommt ein als Laparoskop bezeichnetes Instrument zum Einsatz, das über einen kleinen Hautschnitt in den Bauchraum eingeführt wird und dem Arzt dann einen Blick auf die betroffenen Organe erlaubt.
Die mit dem Laparoskop verbundene Videokamera liefert dabei ein Bildsignal, das sich aus den drei Farbkanälen Rot, Grün und Blau (RGB) zusammensetzt. Dieser Farbraum wird beispielsweise auch bei Fernsehern oder Smartphones genutzt. Es hat sich jedoch gezeigt, dass das Gewebe über optische Eigenschaften verfügt, die sich allein mit diesen Bildinformationen nicht darstellen lassen. Lena Maier-Hein (DKFZ) und ihr Team haben deshalb im Rahmen des vom Europäischen Forschungsrat ERC geförderten Projektes „NEURAL spicing“ gemeinsam mit Forscherinnen und Forschern vom Städtischen Klinikum Karlsruhe den Einsatz multispektraler Bildgebungssysteme untersucht. Die dabei verwendeten Kamerasysteme erfassen nicht nur die genannten drei, sondern insgesamt 16 Wellenlängenbereiche des optischen Spektrums. Dadurch lassen sich bestimmte funktionelle Eigenschaften des Gewebes sichtbar machen, die für herkömmliche Kamerasysteme unsichtbar sind, etwa die Durchblutung eines Organs.
Das ist zum Beispiel bei Patienten mit Nierenkrebs relevant, bei denen der Tumor operativ entfernt werden soll. Bei diesem Eingriff muss zunächst der Blutfluss in die betroffenen Areale durch Abklemmen der Arterien unterbrochen werden. Durch das RGB-Videobild eines herkömmlichen Laparoskops lässt sich die Durchblutung des Gewebes allerdings kaum beurteilen. Erst durch den Einsatz eines fluoreszierenden Kontrastmittels, das dem Patienten gespritzt wird und sich anschließend in den durchbluteten Geweben anreichert, kann der Arzt erkennen, ob die richtigen Segmente des Organs von der Blutzufuhr getrennt wurden. War dies nicht erfolgreich, muss das Kontrastmittel zunächst für etwa 30 Minuten ausgewaschen werden, um den Vorgang anschließend wiederholen zu können.
„Wir konnten zeigen, dass sich die Durchblutung der Niere mit einer Kombination aus multispektraler Bildgebung und Künstlicher Intelligenz auch ohne Kontrastmittel und in Echtzeit darstellen lässt“, sagt Lena Meier-Hein. Die neue Technologie kam nun im Rahmen einer Studie erfolgreich bei zehn Patienten zum Einsatz, bei denen Teile der Niere entfernt werden mussten. „Da sich bei unserem Ansatz die Durchblutung des Gewebes live beobachten lässt, kann das Abklemmen der Blutgefäße bei Bedarf sofort korrigiert werden. Das reduziert die Dauer des Eingriffs und macht ihn dadurch sicherer für die Patientinnen und Patienten“, ergänzt Leonardo Ayala, einer der Erstautoren der Studie. Auch das Risiko einer allergischen Reaktion auf das Kontrastmittel entfällt durch die neue Technologie.
Eine entscheidende Rolle spielen bei diesem Ansatz die Erfassung und Verarbeitung der Bilddaten. Denn der Einsatz multispektraler Bildgebungssysteme in der minimalinvasiven Chirurgie scheiterte bislang unter anderem an der Zeit, die die Systeme für diese beiden Schritte benötigen. Sind jeweils mehrere Sekunden nötig, um ein neues Bild zu berechnen, ist die Information während des Eingriffs praktisch nicht nutzbar. Durch den Einsatz einer neuen multispektralen Kameratechnologie konnten die Forscher dieses Problem nun lösen. Ihr neu entwickeltes System liefern 25 Bilder pro Sekunde und somit ein flüssiges Videobild.
Zudem gelang es dem Team, die Durchblutung erstmals mit Methoden der Künstlichen Intelligenz (KI) zu erfassen, die nicht auf große Mengen von Trainingsdaten angewiesen sind. Die KI lernt stattdessen bei jedem Patienten neu, durchblutetes von nicht-durchblutetem Gewebe zu unterschieden. „Das ist nötig, weil das Gewebe nicht bei jedem Patienten gleich ist, sodass auch die optischen Eigenschaften sehr unterschiedlich sein können“, erklärt Leonardo Ayala. Zu Beginn einer Operation wird deshalb mithilfe des Laparoskops bei jedem Patienten eine kurze Videosequenz von der Niere aufgenommen. „Der Algorithmus berechnet dann auf der Grundlage der individuellen Bilddaten des Patienten, wie sich der Durchblutungsstatus auf die optischen Eigenschaften des Gewebes auswirkt, damit während der Operation der Grad der Durchblutung eines Areals angezeigt werden kann“, so Tim Adler, ebenfalls Erstautor der Studie.
Vergleichbare Verfahren könnten zukünftig auch bei anderen chirurgischen Fragestellungen zum Einsatz kommen. Dogu Teber (Städtisches Klinikum Karlsruhe), klinischer Leiter der Studie, sieht großes Potenzial für diesen neuen technologischen Ansatz: „Die spektrale Bildgebung in Kombination mit neuen KI-basierten Analysetools könnte sich zu einem wichtigen Instrument für die schnelle, zuverlässige und sichere funktionelle Bildgebung in der minimalinvasiven Chirurgie entwickeln.“
Leonardo Ayala, Tim J. Adler, Silvia Seidlitz, Sebastian Wirkert, Christina Engels, Alexander Seitel, Jan Sellner, Alexey Aksenov, Matthias Bodenbach, Pia Bader, Sebastian Baron, Anant Vemuri, Manuel Wiesenfarth, Nicholas Schreck, Diana Mindroc, Minu Tizabi, Sebastian Pirmann, Brittaney Everitt, Annette Kopp-Schneider, Dogu Teber, Lena Maier-Hein: Spectral imaging enables contrast agent-free real-time ischemia monitoring in laparoscopic surgery.
Science Advances (2023) DOI: https://doi.org/10.1101/2022.03.08.22271465
Das Deutsche Krebsforschungszentrum (DKFZ) ist mit mehr als 3.000 Mitarbeiterinnen und Mitarbeitern die größte biomedizinische Forschungseinrichtung in Deutschland. Über 1.300 Wissenschaftlerinnen und Wissenschaftler erforschen im DKFZ, wie Krebs entsteht, erfassen Krebsrisikofaktoren und suchen nach neuen Strategien, die verhindern, dass Menschen an Krebs erkranken. Sie entwickeln neue Methoden, mit denen Tumoren präziser diagnostiziert und Krebspatienten erfolgreicher behandelt werden können.
Beim Krebsinformationsdienst (KID) des DKFZ erhalten Betroffene, interessierte Bürger und Fachkreise individuelle Antworten auf alle Fragen zum Thema Krebs.
Gemeinsam mit Partnern aus den Universitätskliniken betreibt das DKFZ das Nationale Centrum für Tumorerkrankungen (NCT) an den Standorten Heidelberg und Dresden, in Heidelberg außerdem das Hopp-Kindertumorzentrum KiTZ. Im Deutschen Konsortium für Translationale Krebsforschung (DKTK), einem der sechs Deutschen Zentren für Gesundheitsforschung, unterhält das DKFZ Translationszentren an sieben universitären Partnerstandorten. Die Verbindung von exzellenter Hochschulmedizin mit der hochkarätigen Forschung eines Helmholtz-Zentrums an den NCT- und den DKTK-Standorten ist ein wichtiger Beitrag, um vielversprechende Ansätze aus der Krebsforschung in die Klinik zu übertragen und so die Chancen von Krebspatienten zu verbessern. Das DKFZ wird zu 90 Prozent vom Bundesministerium für Bildung und Forschung und zu 10 Prozent vom Land Baden-Württemberg finanziert und ist Mitglied in der Helmholtz-Gemeinschaft Deutscher Forschungszentren.
Deutsches Krebsforschungszentrum
Im Neuenheimer Feld 280
69120 Heidelberg
Telefon: +49 (6221) 420
Telefax: +49 (6221) 422995
http://www.dkfz.de
Presse- und Öffentlichkeitsarbeit
Telefon: +49 (6221) 42-2854
Fax: +49 (6221) 42-2399
E-Mail: presse@dkfz.de
![]()